Усі хімічні речовини поділяються на прості і складні.
Простими називаються речовини, утворені атомами одного хімічного елемента.
Деякі прості речовини складаються з молекул.
Одноатомні молекули утворюють інертні гази гелій He, неон Ne, аргон Ar та інші.
З двохатомних молекул складаються водень H2, кисень O2, азот N2, галогени F2, Cl2, Br2, I2.
Три атоми — у молекулах озону O3, чотири — у молекулах білого фосфору P4, вісім — у молекулах сірки S8.
Моделі молекул водню і азоту
Модель молекули білого фосфору
Інша група простих речовин має немолекулярну будову. До таких речовин відносяться усі метали, а також червоний фосфор, алмаз, графіт, силіцій та інші.
Їх хімічні формули записують хімічним символом елемента без індексу: Fe, P, C, Si, тощо.
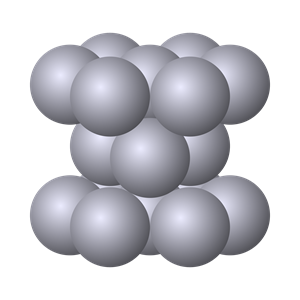
Модель кристалу заліза
Відомо 118 хімічних елементів, а простих речовин — більше, ніж 400. Один хімічний елемент може утворити кілька простих речовин.
Явище існування декількох простих речовин, утворених атомами одного хімічного елемента, називається алотропією.
Прості речовини, що складаються з атомів одного хімічного елемента — алотропні модифікації (алотропні видозміни).
Приклад:
хімічний елемент Оксиген утворює прості речовини, що відрізняються складом молекул: кисень O2 і озон O3. Кисень — газ без запаху, він є необхідним живим організмам для дихання. Озон має запах, отруйний.
Хімічний елемент Фосфор утворює молекулярну речовину — білий фосфор P4 і немолекулярну — червоний фосфор P. Ці речовини відрізняються не лише будовою, а й властивостями. Білий фосфор має запах, самозаймається на повітрі. Червоний фосфор без запаху, горить лише при нагріванні.
Хімічний елемент Карбон утворює немолекулярні речовини алмаз і графіт. Вони позначаються однаковою формулою — C, але мають різну будову і відрізняються властивостями. Алмаз є прозорою, безбарвною, дуже твердою речовиною. Графіт — непрозорий, темно-сірий, м'який.
Алмаз і графіт
Хімічний елемент і проста речовина
Назви хімічного елемента і простої речовини у більшості випадків збігаються, тому слід розрізняти ці два поняття.
Хімічний елемент — це певний вид атомів. Атоми хімічного елемента можуть входити до складу простих і складних речовин. Можна охарактеризувати поширеність і форми знаходження хімічного елемента в природі, а також властивості його атомів (масу, розміри, будову).
Проста речовина — це одна з форм існування хімічного елемента в природі. Проста речовина характеризується певним складом, будовою, фізичними і хімічними властивостями. Її використовують для отримання інших речовин.
Приклад:
Хімічний елемент | Проста речовина |
| Відносна атомна маса Оксигену дорівнює 16 | Кисень погано розчиняється у воді |
| Нітроген входить до складу білків | Азот використовують для отримання аміаку |
| Атоми Гідрогену входять до складу молекул води | Водень легший за повітря |
Хімічні елементи входять до складу складних речовин (хімічних сполук).
Складними називаються речовини, до складу яких входять атоми різних хімічних елементів.
Більшість хімічних речовин є складними.
Багато складних речовин мають молекулярну будову. До молекулярних відносяться метан CH4, вода H2O, вуглекислий газ CO2, сульфатна кислота H2SO4, глюкоза C6H12O6. Пластмаси, білки, жири, крохмаль теж є складними речовинами, що складаються з молекул.
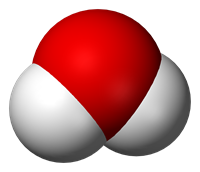
Модель молекули води
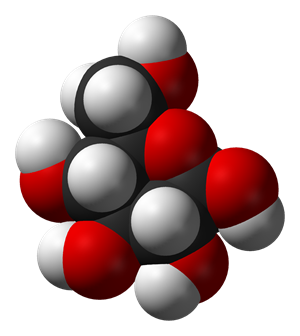
Модель молекули глюкози
Немолекулярну будову мають пісок SiO2, а також усі складні речовини, до складу яких входять метали: кухонна сіль NaCl, крейда CaCO3, питна сода NaHCO3 тощо. Зі складних речовин немолекулярної будови складаються мінерали і гірські породи.
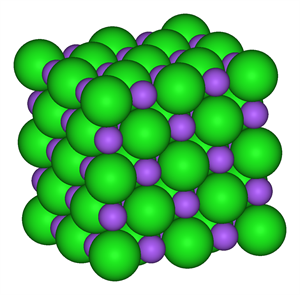
Модель кристала кухонної солі
За певних умов складні речовини можна розкласти на кілька нових речовин. Так, під дією електричного струму вода розкладається на водень і кисень, а цукор при нагріванні перетворюється на вугілля і воду.
Водень і кисень зовсім не схожі на воду. За нормальних умов водень і кисень є газами, а вода — рідина. Вугілля і вода нічим не нагадують цукор.
Властивості складної речовини не є сумою властивостей речовин, що утворюються при її розкладанні.
ДЖЕРЕЛО- https://miyklas.com.ua/p/himija/7-klas/pochatkovi-khimichni-poniattia-39391/prosti-i-skladni-rechovini-39174/re-d186b87b-0de8-441a-9144-a5598f9aec65
ПРОСТІ ТА СКЛАДНІ РЕЧОВИНИ
Якщо хімічних елементів 116, то речовин - понад 10 мільйонів!
Мета вивчення речовин: створення нових та безпечне використання речовин.
ПРОСТІ РЕЧОВИНИ утворені атомами одного хімічного елемента.
Приклади простих речовин: кисень, водень, азот, озон, залізо, графіт, алюміній, сірка.
| Речовина | Хімічна формула, модель | Читаємо | Кількість атомів |
| Кисень | О2 
| «о-два» | два атоми Оксигену |
| Водень | H2 
| «аш-два» | два атоми Гідрогену |
| озон | О3 
| «о-три» | три атоми Оксигену |
| Графіт | C 
| «це» | один атом Карбону |
| Залізо | Fe 
| «ферум» | один атом Феруму |
| Азот | N2 
| «ен-два» | два атоми Нітрогену |
СКЛАДНІ РЕЧОВИНИ утворені з атомів двох і більше хімічних елементів. Атоми різних хімічних елементів здатні сполучатися один з одним у різній кількості та послідовності, тому складних речовин більше, ніж простих.
Приклади складних речовин: вуглекислий газ, вода, метан, пероксид водню, сіль, питна сода, органічні речовини.
| Речовина | Хімічна формула, модель | Читаємо | Кількість атомів |
| Вода | Н2О 
| «аш-два-о» | два атоми Гідрогену та один атом Оксигену |
| Вуглекислий газ | СО2 
| «це-о-два» | один атом Карбону і два атоми Оксигену |
| метан | СН4 
| «це-аш-чотири» | один атом Карбону і чотири атоми Гідрогену |
| Гідроген пероксиду (перекис водню) | H2О2 
| «аш-два-о-два» | два атоми Гідрогену і два атоми Оксигену |
| Органічні речовини (курячий білок, олія, крохмаль, пластмаса, гума, поліетилен) |
Спільні ознаки простих і складних речовин: складаються з хімічних елементів
Відмінні ознаки:
Прості речовини | Складні речовини |
Будуються з атомів одного хімічного елементу | Будуються з атомів двох і більше хімічних елементів |
Не розкладаються з утворенням нових речовин | Розкладаються з утворенням нових речовин |
Поділяють на метали і неметали | Поділяють на органічні та неорганічні |
http://8next.com/pr/3210-pr_10.html